三類體外診斷試劑產(chǎn)品延續(xù)注冊
- 立即咨詢
-
全國服務(wù)熱線:
400-888-7587

注冊認(rèn)證 · 許可備案 · 體系輔導(dǎo) · 企業(yè)培訓(xùn)
400-888-7587
0755-86194173
、13502837139020-82177679、13602603195
四川:028-68214295
湖南:0731-22881823
、15013751550
? 辦理?xiàng)l件 / Conditions
申請人應(yīng)為境內(nèi)依法進(jìn)行登記的企業(yè)
政府官方原文鏈接:
http://samr.cfda.gov.cn/WS01/CL1768/152058.html
? 申請材料清單 / List of application materials
1.申請表
2.明性文件
(1)注冊人企業(yè)營業(yè)執(zhí)照的副本和組織機(jī)構(gòu)代碼證復(fù)印件
3.關(guān)于產(chǎn)品沒有變化的聲明
(1)注冊人提供產(chǎn)品沒有變化的聲明
4.原醫(yī)療器械注冊證及其附件復(fù)印件、歷次醫(yī)療器械注冊變更文件復(fù)印件
5.注冊證有效期內(nèi)產(chǎn)品分析報(bào)告
(1)產(chǎn)品臨床應(yīng)用情況
(2)醫(yī)療器械不良事件匯總分析評(píng)價(jià)報(bào)告,報(bào)告應(yīng)對(duì)醫(yī)療器械上市后發(fā)生的可疑不良事件列表
(3)在所有上市國家和地區(qū)的產(chǎn)品市場情況說明。
(4)產(chǎn)品監(jiān)督抽驗(yàn)情況(如有)
(5)如上市后發(fā)生了召回
(6)原醫(yī)療器械注冊證中載明要求繼續(xù)完成工作的
6.產(chǎn)品檢驗(yàn)報(bào)告
(1)如醫(yī)療器械強(qiáng)制性標(biāo)準(zhǔn)已經(jīng)修訂
,應(yīng)提供產(chǎn)品能夠達(dá)到新要求的產(chǎn)品檢驗(yàn)報(bào)告。產(chǎn)品檢驗(yàn)報(bào)告可以是自檢報(bào)告、委托檢驗(yàn)報(bào)告或符合強(qiáng)制性標(biāo)準(zhǔn)實(shí)施通知規(guī)定的檢驗(yàn)報(bào)告。其中(2)如有國家標(biāo)準(zhǔn)品、參考品發(fā)布或者更新的
7.符合性聲明
(1)注冊人聲明本產(chǎn)品符合《體外診斷試劑注冊管理辦法》和相關(guān)法規(guī)的要求;聲明本產(chǎn)品符合現(xiàn)行國家標(biāo)準(zhǔn)
(2)所提交資料真實(shí)性的自我保證聲明
8.其他
如在原注冊證有效期內(nèi)發(fā)生了涉及產(chǎn)品說明書和/或產(chǎn)品技術(shù)要求變更的
? 辦理流程 / Processing process
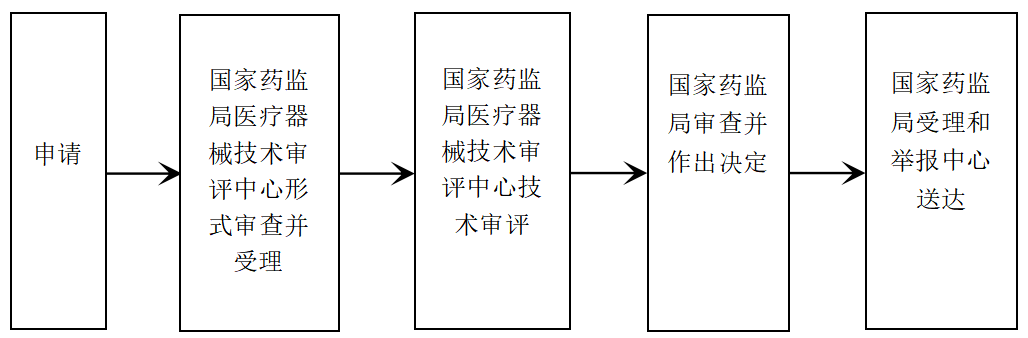
? 廣東政務(wù)局服務(wù)承諾時(shí)間 / Service Commitment Time of Guangdong Government Bureau
名稱 | 解釋說明 | 時(shí)限 |
受理 | 5(工作日) | |
行政許可決定 | 20個(gè)工作日(不含技術(shù)審評(píng)和申請人補(bǔ)充資料及補(bǔ)充資料審評(píng)所需的時(shí)間)。20個(gè)工作日內(nèi)不能做出決定的 | 20(工作日) |
? 辦理依據(jù) / Processing basis
《醫(yī)療器械監(jiān)督管理?xiàng)l例》(國務(wù)院令第650號(hào))第十五條:“醫(yī)療器械注冊證有效期為5年 。有效期屆滿需要延續(xù)注冊的 ,應(yīng)當(dāng)在有效期屆滿6個(gè)月前向原注冊部門提出延續(xù)注冊的申請。除有本條第三款規(guī)定情形外 ,接到延續(xù)注冊申請的食品藥品監(jiān)督管理部門應(yīng)當(dāng)在醫(yī)療器械注冊證有效期屆滿前作出準(zhǔn)予延續(xù)的決定 。逾期未作決定的,視為準(zhǔn)予延續(xù) 。有下列情形之一的 ,不予延續(xù)注冊: 1.注冊人未在規(guī)定期限內(nèi)提出延續(xù)注冊申請的; 2.醫(yī)療器械強(qiáng)制性標(biāo)準(zhǔn)已經(jīng)修訂 ,申請延續(xù)注冊的醫(yī)療器械不能達(dá)到新要求的 ; 3.對(duì)用于治療罕見疾病以及應(yīng)對(duì)突發(fā)公共衛(wèi)生事件急需的醫(yī)療器械,未在規(guī)定期限內(nèi)完成醫(yī)療器械注冊證載明事項(xiàng)的 ?div id="jfovm50" class="index-wrap">!?/p> | 《國家食品藥品監(jiān)督管理總局關(guān)于調(diào)整部分醫(yī)療器械行政審批事項(xiàng)審批程序的決定》(局令第32號(hào)):將下列由國家食品藥品監(jiān)督管理總局作出的醫(yī)療器械行政審批決定,調(diào)整為由國家食品藥品監(jiān)督管理總局醫(yī)療器械技術(shù)審評(píng)中心以國家食品藥品監(jiān)督管理總局名義作出: 一 、第三類高風(fēng)險(xiǎn)醫(yī)療器械臨床試驗(yàn)審批決定 ; 二、國產(chǎn)第三類醫(yī)療器械和進(jìn)口醫(yī)療器械許可事項(xiàng)變更審批決定 ; 三 、國產(chǎn)第三類醫(yī)療器械和進(jìn)口醫(yī)療器械延續(xù)注冊審批決定。 其他醫(yī)療器械注冊申請的審批決定 ,按現(xiàn)程序 ,由國家食品藥品監(jiān)督管理總局作出。 |
? 金飛鷹相關(guān)服務(wù) / Golden Eagle related services
●延續(xù)條件確認(rèn) ●產(chǎn)品分類確定或分類申請 ●創(chuàng)新產(chǎn)品申報(bào) ●產(chǎn)品技術(shù)要求確定 ●廠房規(guī)劃及平面圖設(shè)計(jì) ●廠房設(shè)施驗(yàn)證 ●產(chǎn)品設(shè)計(jì)驗(yàn)證 | ●產(chǎn)品工藝驗(yàn)證 ●產(chǎn)品樣品送檢資料準(zhǔn)備 ●豁免臨床試驗(yàn)產(chǎn)品臨床驗(yàn)證 ●不豁免臨床試驗(yàn)產(chǎn)品臨床試驗(yàn)CRO ●臨床試驗(yàn)方案備案 ●產(chǎn)品注冊資料準(zhǔn)備 ●產(chǎn)品注冊資料遞交 | ●生產(chǎn)現(xiàn)場車間GMP文件編制 ●產(chǎn)品SOP文件編制 ●體系考核輔導(dǎo)與培訓(xùn) ●相關(guān)生產(chǎn)與檢驗(yàn)設(shè)備 、車間環(huán)境檢驗(yàn)儀器等確定 ●GMP體系考核前的預(yù)檢查 ●GMP體系考核后的不符合項(xiàng)改善 ●注冊證進(jìn)度跟蹤 |
? 結(jié)果樣本 / Results the sample
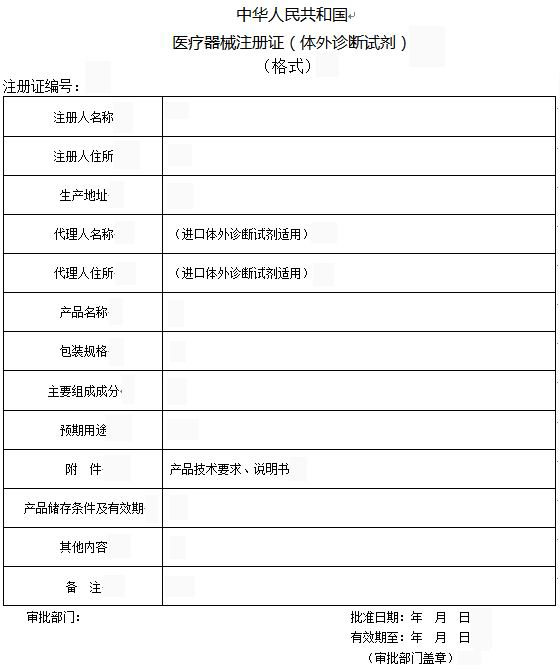
全面解決您的研發(fā)

Team
40多位經(jīng)驗(yàn)豐富的項(xiàng)目專員
practical experience
2000多個(gè)二
Professional translation
匯聚7大語種專業(yè)翻譯精英
Software development
強(qiáng)大的軟件研發(fā)團(tuán)隊(duì)
Group supply chain
嚴(yán)選數(shù)十個(gè)優(yōu)秀的醫(yī)械行業(yè)服務(wù)機(jī)構(gòu)
多次創(chuàng)造二三類高風(fēng)險(xiǎn)產(chǎn)品一次性通過的行業(yè)紀(jì)錄
項(xiàng)目狀態(tài):已結(jié)案
項(xiàng)目輔導(dǎo)老師:李老師
項(xiàng)目狀態(tài):已結(jié)案
項(xiàng)目輔導(dǎo)老師:車?yán)蠋?/p>
項(xiàng)目狀態(tài):已結(jié)案
項(xiàng)目輔導(dǎo)老師:王老師
項(xiàng)目狀態(tài):已結(jié)案
項(xiàng)目輔導(dǎo)老師:黃老師
電話
400-888-7587
0755-86194173
020-82177679、13602603195
微信

微信公眾

小程序
郵箱
617677449@qq.com