專注國內(nèi)外醫(yī)療器械咨詢服務(wù)
注冊認(rèn)證 · 許可備案 · 體系輔導(dǎo) · 企業(yè)培訓(xùn)
400-888-7587
0755-86194173
020-82177679
四川:028-68214295、15718027946
湖南:0731-22881823、15013751550
列表
廣東藥監(jiān)局發(fā)布10項要點,落實醫(yī)療器械【委托生產(chǎn)】主體責(zé)任!
文章出處:公告通知 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時間:2024-02-28
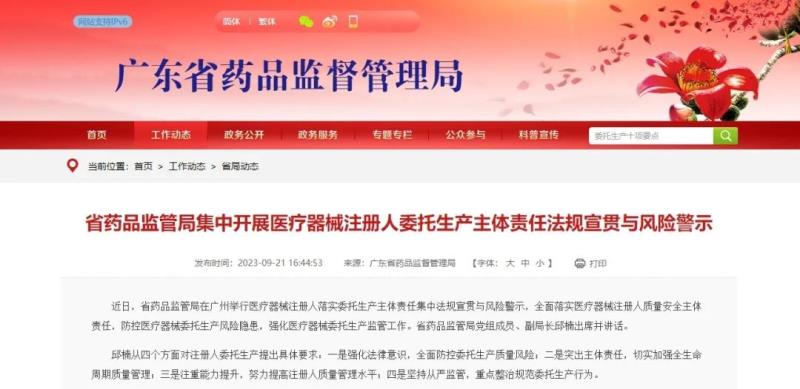
9月21日,廣東藥監(jiān)局官網(wǎng)發(fā)布動態(tài)稱,近日,該局在廣州舉行醫(yī)療器械注冊人落實委托生產(chǎn)主體責(zé)任集中法規(guī)宣貫與風(fēng)險警示,全面落實醫(yī)療器械注冊人質(zhì)量安全主體責(zé)任,防控醫(yī)療器械委托生產(chǎn)風(fēng)險隱患,強(qiáng)化醫(yī)療器械委托生產(chǎn)監(jiān)管工作。
同步公布了一份附件《廣東省醫(yī)療器械注冊人落實委托生產(chǎn)主體責(zé)任十項要點》,具體內(nèi)容如下:
一、注冊人、受托生產(chǎn)企業(yè)均應(yīng)當(dāng)按照《醫(yī)療器械監(jiān)督管理條例》
、《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》及相關(guān)法規(guī)、標(biāo)準(zhǔn),建立健全質(zhì)量管理體系并保持有效運(yùn)行。二、注冊人應(yīng)當(dāng)組織對受托生產(chǎn)企業(yè)生產(chǎn)管理、質(zhì)量管理進(jìn)行首次評估
,確保滿足委托生產(chǎn)要求,并每年對受托生產(chǎn)企業(yè)質(zhì)量管理體系進(jìn)行一次審核,評估其質(zhì)量管理體系的持續(xù)性、有效性。三、注冊人
四 五、受托生產(chǎn)企業(yè)應(yīng)當(dāng)按照注冊人轉(zhuǎn)移的產(chǎn)品技術(shù)資料轉(zhuǎn)化為內(nèi)部執(zhí)行的文件 六、注冊人在受托生產(chǎn)企業(yè)的生產(chǎn)放行完成后,應(yīng)當(dāng)對受托方的生產(chǎn)放行文件進(jìn)行審核 七、注冊人應(yīng)當(dāng)切實履行不良事件監(jiān)測主體責(zé)任 八、注冊人應(yīng)當(dāng)按照《企業(yè)落實醫(yī)療器械質(zhì)量安全主體責(zé)任監(jiān)督管理規(guī)定》要求 九、注冊人應(yīng)當(dāng)充分履行產(chǎn)品風(fēng)險管理、變更控制 十、注冊人不再進(jìn)行醫(yī)療器械生產(chǎn)和經(jīng)營活動的 ,快?來跟我漲姿勢!" linktype="text" imgurl="" imgdata="null" data-itemshowtype="0" tab="innerlink" data-linktype="2" hasload="1" style="margin: 0px; padding: 0px; outline: 0px; text-decoration-line: none; -webkit-tap-highlight-color: rgba(0, 0, 0, 0); -webkit-user-drag: none; cursor: pointer; max-width: 100%; box-sizing: border-box !important; overflow-wrap: break-word !important;">√激光治療設(shè)備分類科普


