專注國內外醫(yī)療器械咨詢服務
注冊認證 · 許可備案 · 體系輔導 · 企業(yè)培訓
400-888-7587
0755-86194173
020-82177679、13602603195
四川:028-68214295
湖南:0731-22881823、15013751550
列表
《醫(yī)用無針注射器注冊審查指導原則》等4項指導原則發(fā)布!
文章出處:公告通知
網(wǎng)責任編輯:
金飛鷹
閱讀量:
發(fā)表時間:2024-02-29
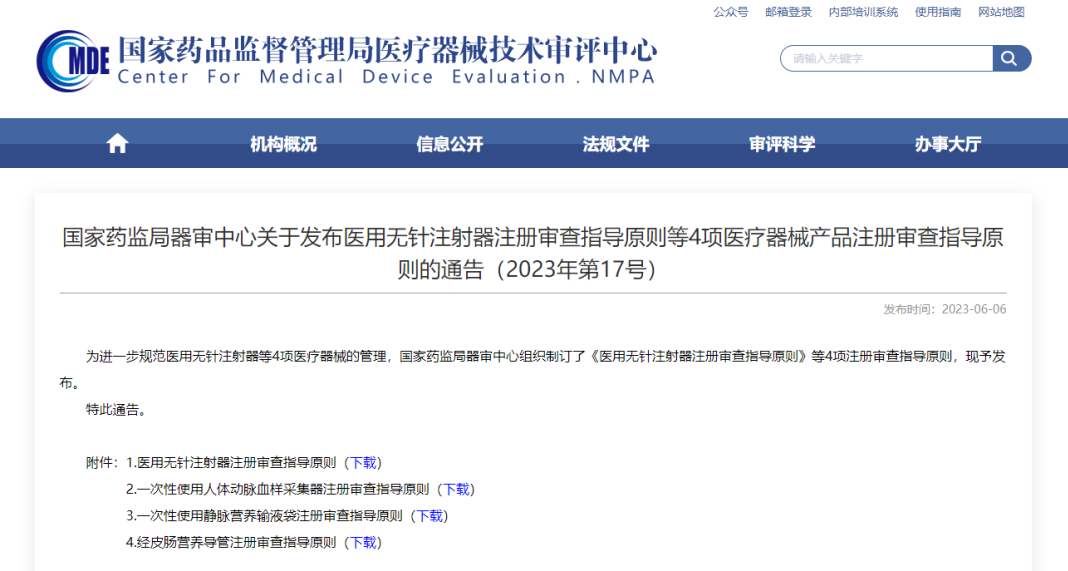
6月6日,國家藥監(jiān)局器審中心官網(wǎng)發(fā)布《醫(yī)用無針注射器注冊審查指導原則》、《一次性使用人體動脈血樣采集器注冊審查指導原則》等4項醫(yī)療器械產品注冊審查指導原則,我們將其中《醫(yī)用無針注射器注冊審查指導原則》部分重點內容摘錄如下:
01 適用范圍
本指導原則適用于依靠壓力發(fā)揮無針注射功能的醫(yī)用無針注射器產品的注冊。醫(yī)用無針注射器用于藥物的注射,通過機械動能(如活塞的運動,不排除其他運動方式)將動態(tài)能量分配傳遞至藥物,使藥物穿透皮膚表面,將藥物輸送入體內。機械動能通常通過壓縮彈簧獲得。醫(yī)用無針注射器產品通常由推動器、藥管和取藥接口組成。推動器通?div id="jfovm50" class="index-wrap">?芍貜褪褂?div id="jfovm50" class="index-wrap">,藥管和取藥接口是一次性使用的產品,不含藥物。
本指導原則不適用于預充有藥物的無針注射器、依靠電能或其他能源發(fā)揮作用的無針注射器。
02 綜述資料-產品描述
產品描述應全面、詳細,需包括但不局限于申報產品名稱、結構組成(包括相應圖示及尺寸,如液體路徑、藥管、劑量設定裝置等)、工作原理、產品各部件發(fā)揮的功能、各部件所用原材料、技術性能指標、使用方法、適用的注射部位及組織深度(例如皮下注射、肌肉注射、皮內注射)、預期用途、滅菌方式、有效期、區(qū)別于已上市其他同類產品的特征等。
明確產品原材料的化學名稱、商品名/材料代號、化學結構式/分子式、供應商名稱、生產商名稱等信息。
需結合醫(yī)用無針注射器產品的具體性能、臨床應用等說明各部件所用原材料的選擇依據(jù)。需提供所用原材料適合用于產品預期臨床用途的相關研究資料,如材料安全性數(shù)據(jù)表、相關毒理學數(shù)據(jù)、臨床應用史等以說明各原材料的安全性、有效性。原材料需具有穩(wěn)定的供貨渠道以保證產品質量,需提供所用原材料符合質量控制標準的研究資料。
03 非臨床資料-產品技術要求
產品技術要求的制定需符合《醫(yī)療器械產品技術要求編寫指導原則》的要求,需根據(jù)產品的技術特征和臨床使用情況來確定產品安全有效、質量可控的技術指標與檢驗方法。對宣稱的產品的技術參數(shù)和功能,需在產品技術要求中予以規(guī)定。
技術指標需不低于相關的國家標準和行業(yè)標準,如YY/T 0907《醫(yī)用無針注射器 要求及試驗方法》。檢驗方法宜優(yōu)先采用國家標準、行業(yè)標準中的方法,若采用其他方法則需說明合理性原因并在研究資料中提供驗證資料。對于相關國家標準、行業(yè)標準中不適用的條款,需說明不適用的原因。
常見的技術指標需包括以下內容但不限于此:
1)根據(jù)YY/T 0907《醫(yī)用無針注射器 要求及試驗方法》制定的技術指標
,如通用要求、噪聲要求、劑量刻度要求、性能要求(如壓力 、速度、注射所需時間 、注射深度和偏差 、機械力、機械動能 、射流沖擊力等) 、測試要求等 。
2)產品尺寸要求
如推動器尺寸、藥管及藥管噴孔直徑
、藥管公稱容量 、取藥接口尺寸等。
3)藥管耐壓性
、密合性 、藥液殘留量、潤滑劑殘留量 。
4)各組件間的適配性
如藥管
、取藥接口與推動器的適配性等。
5)化學性能
如可萃取金屬含量
、酸堿度、易氧化物、環(huán)氧乙烷殘留等。
6)其他性能
如無菌、細菌內毒素等
。
申請人還可根據(jù)產品具體特點及在臨床上所需達到的性能
,制訂其他相應的技術指標要求。
以上就是我們整理的《醫(yī)用無針注射器注冊審查指導原則》部分重點內容啦,如需查看本次發(fā)布的4項指導原則全文,請點擊文末“閱讀原文”。
往期精彩推薦 # #
文章出處:公告通知 網(wǎng)責任編輯: 金飛鷹 閱讀量: 發(fā)表時間:2024-02-29

6月6日 本指導原則適用于依靠壓力發(fā)揮無針注射功能的醫(yī)用無針注射器產品的注冊 本指導原則不適用于預充有藥物的無針注射器 產品描述應全面 明確產品原材料的化學名稱 需結合醫(yī)用無針注射器產品的具體性能、臨床應用等說明各部件所用原材料的選擇依據(jù) 產品技術要求的制定需符合《醫(yī)療器械產品技術要求編寫指導原則》的要求,需根據(jù)產品的技術特征和臨床使用情況來確定產品安全有效 技術指標需不低于相關的國家標準和行業(yè)標準 常見的技術指標需包括以下內容但不限于此: 1)根據(jù)YY/T 0907《醫(yī)用無針注射器 要求及試驗方法》制定的技術指標 2)產品尺寸要求 如推動器尺寸、藥管及藥管噴孔直徑 3)藥管耐壓性 4)各組件間的適配性 如藥管 5)化學性能 如可萃取金屬含量 6)其他性能 如無菌、細菌內毒素等 申請人還可根據(jù)產品具體特點及在臨床上所需達到的性能 以上就是我們整理的《醫(yī)用無針注射器注冊審查指導原則》部分重點內容啦


