專注國(guó)內(nèi)外醫(yī)療器械咨詢服務(wù)
注冊(cè)認(rèn)證 · 許可備案 · 體系輔導(dǎo) · 企業(yè)培訓(xùn)
400-888-7587
0755-86194173
020-82177679、13602603195
四川:028-68214295
湖南:0731-22881823
列表
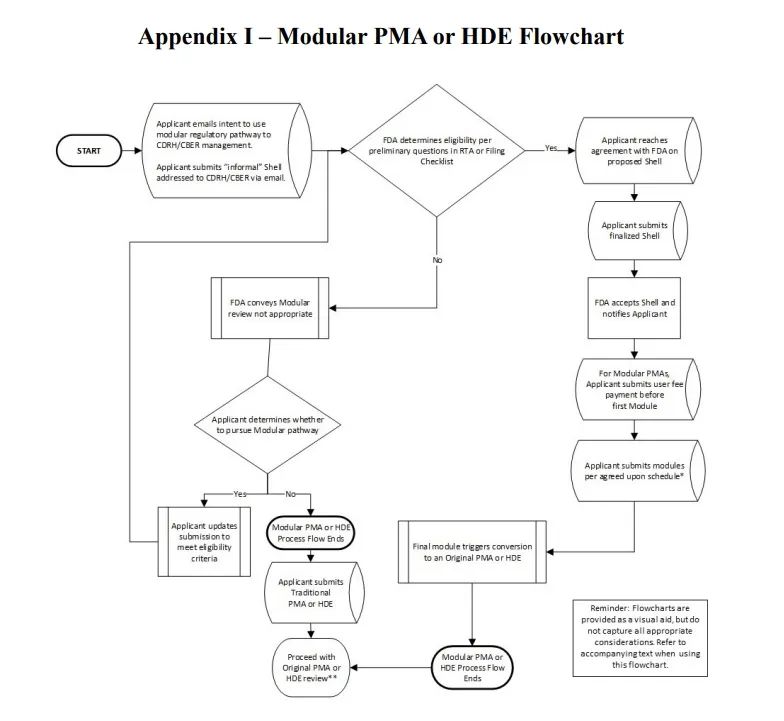
FDA發(fā)布PMA&HDE模塊化審核指南文件
文章出處:法規(guī)動(dòng)態(tài) 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時(shí)間:2025-01-15

美國(guó)當(dāng)?shù)貢r(shí)間1月13日,F(xiàn)DA發(fā)布了上市前批準(zhǔn)申請(qǐng)(PMA)和人道主義器械豁免(HDE)模塊審查的最終文件Premarket Approval Application and Humanitarian Device Exemption Modular Review FDA的模塊化審查指南為醫(yī)療器械的審批提供了一種新的 指南文件附錄1中提到的模塊化審核流程圖如下: 總的來(lái)說(shuō) 醫(yī)療器械注冊(cè)咨詢認(rèn)準(zhǔn)金飛鷹 深圳:0755-86194173 廣州:020 - 82177679 四川:028 - 68214295 湖南:0731-22881823 湖北:181-3873-5940 江蘇:135-5494-7827 廣西:188-2288-8311 海南:135-3810-3052 重慶:135-0283-7139