專注國(guó)內(nèi)外醫(yī)療器械咨詢服務(wù)
注冊(cè)認(rèn)證 · 許可備案 · 體系輔導(dǎo) · 企業(yè)培訓(xùn)
400-888-7587
0755-86194173
020-82177679、13602603195
四川:028-68214295、15718027946
湖南:0731-22881823
列表
√簡(jiǎn)明易懂!韓國(guó)醫(yī)療器械注冊(cè)要點(diǎn)全解析
文章出處:行業(yè)干貨
網(wǎng)責(zé)任編輯:
金飛鷹
閱讀量:
發(fā)表時(shí)間:2024-02-26
導(dǎo)語(yǔ) 金飛鷹醫(yī)療器械國(guó)外注冊(cè)系列文章,繼新加坡、日本、沙特、泰國(guó)后,今天給大家?guī)?lái)的是——韓國(guó)。
作為發(fā)達(dá)國(guó)家中的一員,韓國(guó)的醫(yī)療器械市場(chǎng)規(guī)模是不可小覷的,然而與美國(guó)等其他發(fā)達(dá)國(guó)家相比,目前韓國(guó)醫(yī)療器械產(chǎn)業(yè)的國(guó)際競(jìng)爭(zhēng)力仍處于較低水平,相關(guān)數(shù)據(jù)顯示,其國(guó)內(nèi)半數(shù)以上的獲準(zhǔn)醫(yī)療器械都源于韓國(guó)境外的國(guó)家。那么本期文章我們就來(lái)跟大家分享一下韓國(guó)醫(yī)療器械注冊(cè)的相關(guān)知識(shí)。
PART.01 分類規(guī)則
韓國(guó)根據(jù)產(chǎn)品對(duì)人體的潛在危害:1)與人體接觸的持續(xù)時(shí)間;2)侵入性程度;3)是否向患者提供藥品或能量;4)是否對(duì)患者有生物學(xué)影響,將醫(yī)療器械分為Ⅰ、Ⅱ、Ⅲ、Ⅳ四個(gè)風(fēng)險(xiǎn)等級(jí)。
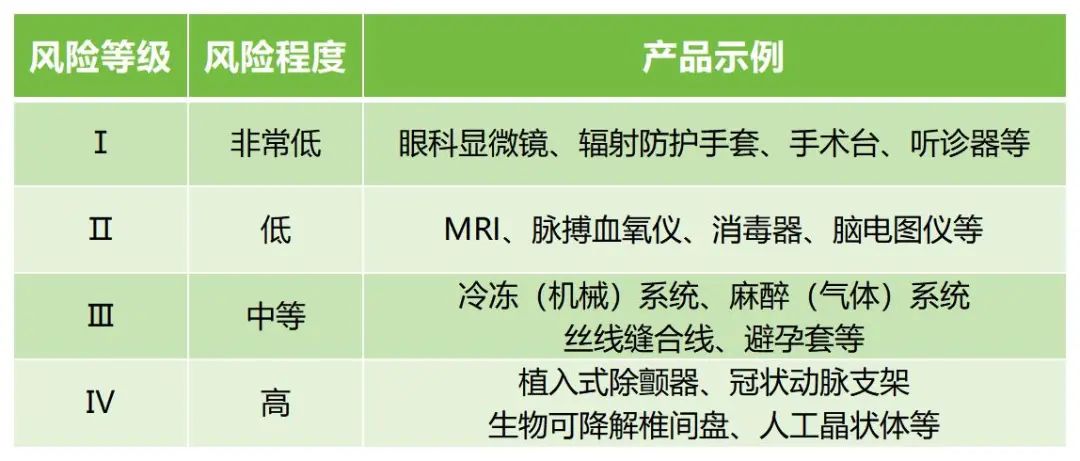
↑ 具體產(chǎn)品示例
可通過(guò)如下方法確定產(chǎn)品分類:
1. 查閱Regulation on Medical Device Groups and Class by Group的Attachment,法規(guī)中規(guī)定了分類規(guī)則以及產(chǎn)品的代碼和風(fēng)險(xiǎn)等級(jí),可以根據(jù)產(chǎn)品定義/用途等判斷產(chǎn)品的等級(jí),我們隨附了示例圖,紅框的數(shù)字為產(chǎn)品的風(fēng)險(xiǎn)等級(jí)。
2. 在韓國(guó)已注冊(cè)產(chǎn)品的數(shù)據(jù)庫(kù)(可聯(lián)系我們獲取鏈接)中
,用產(chǎn)品名稱(英文/韓文)進(jìn)行檢索,查找類似產(chǎn)品在MFDS中的分類。
上述方法需一并查詢以確定產(chǎn)品在韓國(guó)的分類
。當(dāng)然,您也可以直接聯(lián)系我們幫您查詢~
PART.02 上市前遞交路徑
在韓國(guó),Ⅰ類產(chǎn)品一般只需在系統(tǒng)上做簡(jiǎn)單的Notification登記即可,有SE Device(即實(shí)質(zhì)等同產(chǎn)品)的Ⅱ類產(chǎn)品,需遞交技術(shù)資料進(jìn)行NIDS認(rèn)證;而對(duì)于NSE Device(即沒(méi)有實(shí)質(zhì)等同產(chǎn)品)的Ⅱ類產(chǎn)品以及Ⅲ、Ⅳ類產(chǎn)品,則需要由MFDS批準(zhǔn)。不同類別產(chǎn)品所需提交的注冊(cè)資料不同,具體可聯(lián)系我們咨詢。
PART.03 韓國(guó)代理人
和大部分國(guó)家或地區(qū)一樣,在韓國(guó)沒(méi)有實(shí)體辦公場(chǎng)所的公司必須任命一名韓國(guó)許可持有人(Korean License Holder)來(lái)協(xié)調(diào)他們向MFDS注冊(cè)醫(yī)療器械的事務(wù)。KLH控制醫(yī)療器械注冊(cè)并幫助韓國(guó)境外制造商遵守韓國(guó)良好生產(chǎn)規(guī)范(KGMP)要求,并且其名字會(huì)出現(xiàn)在制造商的MFDS醫(yī)療器械注冊(cè)證書(產(chǎn)品審批證書)上。產(chǎn)品獲批后,KLH需負(fù)責(zé)進(jìn)口醫(yī)療器械的年度報(bào)告事宜,并且接受MFDS的突擊審核。
一般情況下,企業(yè)會(huì)選擇在韓國(guó)的分銷商作為證書持證人,但選擇沒(méi)有銷售合作并有能力協(xié)助產(chǎn)品注冊(cè)的韓國(guó)企業(yè)作為持證人,在后續(xù)需要更換經(jīng)銷商時(shí)可能會(huì)更加便捷。
PART.04 質(zhì)量體系要求
在韓國(guó),Ⅱ、Ⅲ、Ⅳ類醫(yī)療器械的制造商都需要符合KGMP(Korean Good Manufacturing Practice)的要求,KGMP要求與ISO 13485類似。
KGMP證書是頒發(fā)給進(jìn)口商(Importor)而不是制造商(Manufacturer), 證書每3年需更新一次,企業(yè)要在在證書過(guò)期前的90天更新。
通常對(duì)于高風(fēng)險(xiǎn)的Ⅲ 、Ⅳ類醫(yī)療器械,由監(jiān)管當(dāng)局MFDS審核制造商的質(zhì)量管理體系 ,而Ⅱ類和部分Ⅲ 、Ⅳ類的醫(yī)療器械交由第三方機(jī)構(gòu)審核。
審核現(xiàn)場(chǎng)的語(yǔ)言要求是韓語(yǔ) ,因此企業(yè)需要提前準(zhǔn)備韓語(yǔ)翻譯 。審核周期大約在9-12個(gè)月。
往期精彩推薦
# ,快?來(lái)跟我漲姿勢(shì)!" linktype="text" imgurl="" imgdata="null" data-itemshowtype="0" tab="innerlink" data-linktype="2" hasload="1" style="margin: 0px; padding: 0px; outline: 0px; text-decoration-line: none; -webkit-tap-highlight-color: rgba(0, 0, 0, 0); -webkit-user-drag: none; cursor: pointer; max-width: 100%; box-sizing: border-box !important; overflow-wrap: break-word !important;">√激光治療設(shè)備分類科普,快來(lái)跟我漲姿勢(shì)!# #
文章出處:行業(yè)干貨 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時(shí)間:2024-02-26
金飛鷹醫(yī)療器械國(guó)外注冊(cè)系列文章,繼新加坡 作為發(fā)達(dá)國(guó)家中的一員,韓國(guó)的醫(yī)療器械市場(chǎng)規(guī)模是不可小覷的 韓國(guó)根據(jù)產(chǎn)品對(duì)人體的潛在危害:1)與人體接觸的持續(xù)時(shí)間;2)侵入性程度;3)是否向患者提供藥品或能量;4)是否對(duì)患者有生物學(xué)影響,將醫(yī)療器械分為Ⅰ、Ⅱ、Ⅲ、Ⅳ四個(gè)風(fēng)險(xiǎn)等級(jí)。 ↑ 具體產(chǎn)品示例 1. 查閱Regulation on Medical Device Groups and Class by Group的Attachment,法規(guī)中規(guī)定了分類規(guī)則以及產(chǎn)品的代碼和風(fēng)險(xiǎn)等級(jí),可以根據(jù)產(chǎn)品定義/用途等判斷產(chǎn)品的等級(jí) 2. 在韓國(guó)已注冊(cè)產(chǎn)品的數(shù)據(jù)庫(kù)(可聯(lián)系我們獲取鏈接)中 上述方法需一并查詢以確定產(chǎn)品在韓國(guó)的分類 在韓國(guó),Ⅰ類產(chǎn)品一般只需在系統(tǒng)上做簡(jiǎn)單的Notification登記即可 和大部分國(guó)家或地區(qū)一樣,在韓國(guó)沒(méi)有實(shí)體辦公場(chǎng)所的公司必須任命一名韓國(guó)許可持有人(Korean License Holder)來(lái)協(xié)調(diào)他們向MFDS注冊(cè)醫(yī)療器械的事務(wù) 一般情況下 在韓國(guó) KGMP證書是頒發(fā)給進(jìn)口商(Importor)而不是制造商(Manufacturer), 證書每3年需更新一次,企業(yè)要在在證書過(guò)期前的90天更新 通常對(duì)于高風(fēng)險(xiǎn)的Ⅲ 審核現(xiàn)場(chǎng)的語(yǔ)言要求是韓語(yǔ) ,快?來(lái)跟我漲姿勢(shì)!" linktype="text" imgurl="" imgdata="null" data-itemshowtype="0" tab="innerlink" data-linktype="2" hasload="1" style="margin: 0px; padding: 0px; outline: 0px; text-decoration-line: none; -webkit-tap-highlight-color: rgba(0, 0, 0, 0); -webkit-user-drag: none; cursor: pointer; max-width: 100%; box-sizing: border-box !important; overflow-wrap: break-word !important;">√激光治療設(shè)備分類科普

![]()


