法規(guī)動態(tài)
您的位置:首頁新聞資訊法規(guī)動態(tài)

注冊認(rèn)證 · 許可備案 · 體系輔導(dǎo) · 企業(yè)培訓(xùn)
400-888-7587
0755-86194173
020-82177679
四川:028-68214295、15718027946
湖南:0731-22881823
您的位置:首頁新聞資訊法規(guī)動態(tài)
文章出處:法規(guī)動態(tài) 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時間:2025-07-23
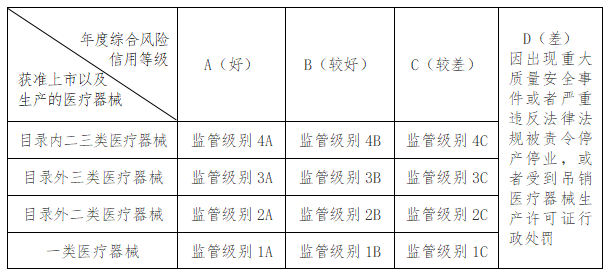
7月21日 我們將《實(shí)施細(xì)則》正文內(nèi)容轉(zhuǎn)載如下: 第一章 總 則 第一條 為加強(qiáng)醫(yī)療器械生產(chǎn)監(jiān)督管理,切實(shí)落實(shí)監(jiān)管責(zé)任,合理配置監(jiān)管資源,保障醫(yī)療器械安全有效,根據(jù)《醫(yī)療器械監(jiān)督管理?xiàng)l例》《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》《國家藥監(jiān)局綜合司關(guān)于加強(qiáng)醫(yī)療器械生產(chǎn)經(jīng)營分級監(jiān)管工作的指導(dǎo)意見》等規(guī)定,制定本實(shí)施細(xì)則。 第二條 本實(shí)施細(xì)則適用于對本市醫(yī)療器械生產(chǎn)企業(yè)開展的日常監(jiān)督管理活動,所稱生產(chǎn)企業(yè)包括醫(yī)療器械注冊人、備案人以及受托生產(chǎn)企業(yè)。 第三條 市藥品監(jiān)管局根據(jù)企業(yè)獲準(zhǔn)上市生產(chǎn)的醫(yī)療器械管理類別、產(chǎn)品是否納入重點(diǎn)監(jiān)管品種目錄、企業(yè)生產(chǎn)質(zhì)量管理體系運(yùn)行狀況、監(jiān)管信用記錄等,按照“風(fēng)險(xiǎn)分級、科學(xué)監(jiān)管,全面覆蓋、動態(tài)調(diào)整,落實(shí)責(zé)任 第四條 市藥品監(jiān)管局負(fù)責(zé)擬制《上海市醫(yī)療器械生產(chǎn)重點(diǎn)監(jiān)管品種目錄》(以下簡稱《市級目錄》) 第二章 監(jiān)管級別的劃分 第五條 根據(jù)國家《醫(yī)療器械生產(chǎn)重點(diǎn)監(jiān)管品種目錄》(以下簡稱《國家級目錄》)和《市級目錄》 (一)一類醫(yī)療器械:獲準(zhǔn)備案或生產(chǎn)的品種涉及第一類醫(yī)療器械; (二)目錄外二類醫(yī)療器械:獲準(zhǔn)注冊或者生產(chǎn)的品種涉及除《國家級目錄》或《市級目錄》外其他第二類醫(yī)療器械; (三)目錄外三類醫(yī)療器械:獲準(zhǔn)注冊或者生產(chǎn)的品種涉及除《國家級目錄》或《市級目錄》外其他第三類醫(yī)療器械; (四)目錄內(nèi)二三類醫(yī)療器械:獲準(zhǔn)注冊或者生產(chǎn)的品種涉及《國家級目錄》或《市級目錄》所列第二類、第三類醫(yī)療器械。 同一醫(yī)療器械生產(chǎn)企業(yè)獲準(zhǔn)上市或生產(chǎn)的醫(yī)療器械產(chǎn)品涉及多種情形的,按照最高情形進(jìn)行劃分。 第六條 根據(jù)本市醫(yī)療器械生產(chǎn)企業(yè)年度綜合風(fēng)險(xiǎn)信用評定情況(評定指標(biāo)詳見附件,市藥品監(jiān)管局可結(jié)合監(jiān)管實(shí)際適時調(diào)整評定指標(biāo)),將企業(yè)劃分為A、B、C、D四個等級。 (一)A級企業(yè)表明其生產(chǎn)質(zhì)量管理體系運(yùn)行狀況及監(jiān)管信用記錄好; (二)B級企業(yè)表明其生產(chǎn)質(zhì)量管理體系運(yùn)行狀況及監(jiān)管信用記錄較好; (三)C級企業(yè)表明其生產(chǎn)質(zhì)量管理體系運(yùn)行狀況及監(jiān)管信用記錄較差; (四)因出現(xiàn)重大質(zhì)量安全事件或者嚴(yán)重違反法律法規(guī)被責(zé)令停產(chǎn)停業(yè),或者受到吊銷醫(yī)療器械生產(chǎn)許可證行政處罰的企業(yè)為D級企業(yè),表明其質(zhì)量管理體系運(yùn)行狀況及監(jiān)管信用記錄差。 第七條 根據(jù)本市醫(yī)療器械生產(chǎn)企業(yè)獲準(zhǔn)上市以及生產(chǎn)的醫(yī)療器械情形、企業(yè)年度綜合風(fēng)險(xiǎn)信用等級,監(jiān)管級別劃分為以下類別。 第三章 日常檢查頻次的確定 第八條 監(jiān)管級別為4A、4B、4C的企業(yè),原則上每年至少組織一次全項(xiàng)目檢查。 第九條 監(jiān)管級別為3A的企業(yè),原則上每兩年全項(xiàng)目檢查不少于一次;監(jiān)管級別為3B、3C的企業(yè),原則上每年檢查不少于一次且每兩年全項(xiàng)目檢查不少于一次。 第十條 監(jiān)管級別為2A、2B、2C的企業(yè),原則上每兩年檢查不少于一次。 第十一條 監(jiān)管級別為1A 第十二條 對于年度綜合風(fēng)險(xiǎn)信用等級為D的企業(yè),如屬于被責(zé)令停產(chǎn)停業(yè),監(jiān)管部門應(yīng)當(dāng)持續(xù)跟蹤企業(yè)整改情況,并在企業(yè)提出復(fù)產(chǎn)申請后開展全項(xiàng)目檢查;通過檢查的企業(yè)方可恢復(fù)生產(chǎn),并在下一年度至少組織一次全項(xiàng)目檢查。 第十三條 市藥品監(jiān)管局根據(jù)上級監(jiān)管要求和監(jiān)管形勢需要,每年確定重點(diǎn)監(jiān)管情形(包括重點(diǎn)監(jiān)管企業(yè)類型、重點(diǎn)監(jiān)管品種),有重點(diǎn)監(jiān)管情形的相關(guān)企業(yè)原則上不減少日常檢查頻次。 對于監(jiān)管級別為4A且無重點(diǎn)監(jiān)管情形的企業(yè),可酌情減少日常檢查頻次,每兩年全項(xiàng)目檢查不少于一次。 對于監(jiān)管級別為3A且無重點(diǎn)監(jiān)管情形的企業(yè),可酌情減少日常檢查頻次,每三年全項(xiàng)目檢查不少于一次。 對于監(jiān)管級別為2A或2B且無重點(diǎn)監(jiān)管情形的企業(yè),可酌情減少日常檢查頻次,每三年檢查不少于一次。 第十四條 對于因未參加上一年度綜合風(fēng)險(xiǎn)信用評定而無法確定監(jiān)管級別的本市醫(yī)療器械生產(chǎn)企業(yè),依照《國家藥監(jiān)局綜合司關(guān)于加強(qiáng)醫(yī)療器械生產(chǎn)經(jīng)營分級監(jiān)管工作的指導(dǎo)意見》,明確相應(yīng)監(jiān)督檢查形式、日常檢查頻次和覆蓋率要求。 第四章 日常檢查頻次的調(diào)整 第十五條 對于當(dāng)年存在以下任何一種情形的本市醫(yī)療器械生產(chǎn)企業(yè),各級監(jiān)管部門可酌情在下一年度增加日常檢查頻次: (一)發(fā)生特別重大或重大醫(yī)療器械安全突發(fā)事件; (二)責(zé)令停產(chǎn); (三)責(zé)令召回; (四)涉及醫(yī)療器械安全有效性的監(jiān)督抽檢不合格 (五)未對醫(yī)療器械不良事件(死亡或嚴(yán)重)采取有效控制措施 (六)新增列入《國家級目錄》或《市級目錄》的醫(yī)療器械 (七)新增國家集中帶量采購中選醫(yī)療器械; (八)新增創(chuàng)新醫(yī)療器械 (九)存在較多舉報(bào)辦件且已查實(shí)存在違法違規(guī)行為 (十)發(fā)生負(fù)面輿情; (十一)屬于不具備生產(chǎn)能力的醫(yī)療器械注冊人 (十二)屬于僅受托生產(chǎn)醫(yī)療器械的企業(yè) (十三)連續(xù)兩年及以上綜合風(fēng)險(xiǎn)信用等級為C級 (十四)其他可以增加日常檢查頻次的情況 第十六條 對于連續(xù)兩年綜合風(fēng)險(xiǎn)信用等級保持A級的本市醫(yī)療器械生產(chǎn)企業(yè) 第十七條 發(fā)生傳染病 第五章 檢查工作要求 第十八條 各級監(jiān)管部門應(yīng)當(dāng)按照年度監(jiān)管計(jì)劃,綜合運(yùn)用多種形式的檢查強(qiáng)化監(jiān)督管理 對本市醫(yī)療器械生產(chǎn)企業(yè)開展的全項(xiàng)目檢查,是指按照醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范及相應(yīng)附錄,對監(jiān)管對象開展覆蓋全部適用項(xiàng)目的檢查,可包括對受托生產(chǎn)企業(yè)相應(yīng)生產(chǎn)活動的檢查。 第十九條 結(jié)合落實(shí)本市藥品監(jiān)管部門規(guī)范涉企行政檢查有關(guān)要求 第二十條 各級監(jiān)管部門可自行組織、聯(lián)合或委托受托生產(chǎn)企業(yè)所在地藥品監(jiān)督管理部門 第二十一條 各級監(jiān)管部門在開展監(jiān)督檢查過程中 第二十二條 本實(shí)施細(xì)則未盡事宜,按照國家藥品監(jiān)督管理局相關(guān)規(guī)定執(zhí)行 第二十三條 本實(shí)施細(xì)則自2025年8月21日起實(shí)施 以上僅對《實(shí)施細(xì)則》正文內(nèi)容進(jìn)行轉(zhuǎn)載 信息來源:上海市藥監(jiān)局 排版整理:金飛鷹藥械 ? 河北藥監(jiān)局抽檢:中頻電療儀等10批次產(chǎn)品不符合標(biāo)準(zhǔn)規(guī)定 ? ,廣州一公司被罰42萬!" data-itemshowtype="0" linktype="text" data-linktype="2" style="-webkit-tap-highlight-color: rgba(0, 0, 0, 0); margin: 0px; padding: 0px; outline: 0px; text-decoration-line: none; -webkit-user-drag: none; cursor: default; max-width: 100%; box-sizing: border-box !important; overflow-wrap: break-word !important;">未經(jīng)審查發(fā)布醫(yī)療器械&處方藥廣告 ? 全國首個醫(yī)療機(jī)構(gòu)應(yīng)用UDI【地方標(biāo)準(zhǔn)】在此落地