列表
一文弄懂→泰國醫(yī)療器械注冊簡明指南
文章出處:企業(yè)原創(chuàng) 網(wǎng)責任編輯: 金飛鷹 閱讀量: 發(fā)表時間:2024-02-28
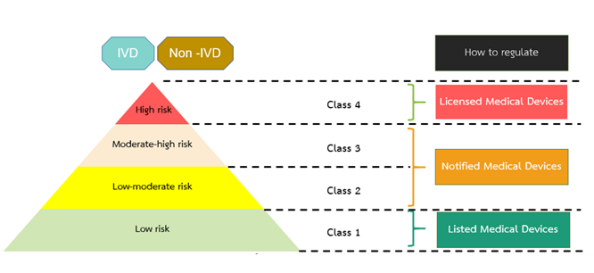
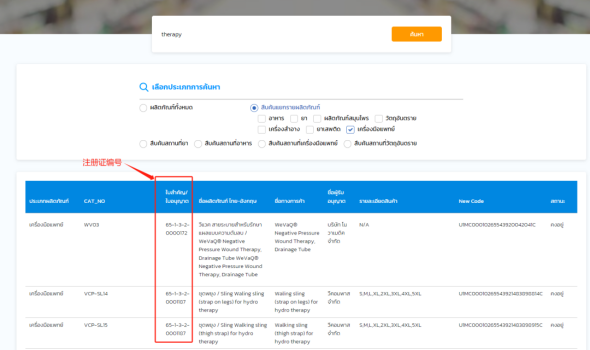
金飛鷹醫(yī)療器械國外注冊系列文章,繼新加坡、日本、沙特后 在“一帶一路”戰(zhàn)略的引領下,東南亞醫(yī)械市場成為我國醫(yī)療器械行業(yè)新的出口增長點 1. 查閱Risk classification of medical devices, B.E. 2562 (2019) 中提到的醫(yī)療器械/體外診斷試劑7條分類規(guī)則 2. 利用官網(wǎng)上的決策小工具You can check your devices' risk classification here by answering a few questions進行查詢(具體網(wǎng)址可聯(lián)系我們獲取) 3. 在TFDA數(shù)據(jù)庫Health Product Search中 【小知識點】:泰國醫(yī)療器械產(chǎn)品注冊證編號的第三個數(shù)字為產(chǎn)品分類 在泰國 另外 確定產(chǎn)品在泰國屬于醫(yī)療器械及相應的產(chǎn)品類別后 針對泰國當?shù)卮恚?/span>Medical Devices Act, B.E.2551 (2008) and (No. 2), B.E. 2562 (2019)的Section 16列出了11條要求,我們將其中前4條列舉如下: 1. (申請medical device establishment的)企業(yè)所有人 2. 不低于20歲 3. 在泰國擁有住所 4. 沒有破產(chǎn) …… 以上就是我們本期分享的泰國醫(yī)療器械注冊的基本知識點 ,快?來跟我漲姿勢