專注國內(nèi)外醫(yī)療器械咨詢服務(wù)
注冊(cè)認(rèn)證 · 許可備案 · 體系輔導(dǎo) · 企業(yè)培訓(xùn)
400-888-7587
0755-86194173、13502837139、19146449057
020-82177679
四川:028-68214295
湖南:0731-22881823
列表
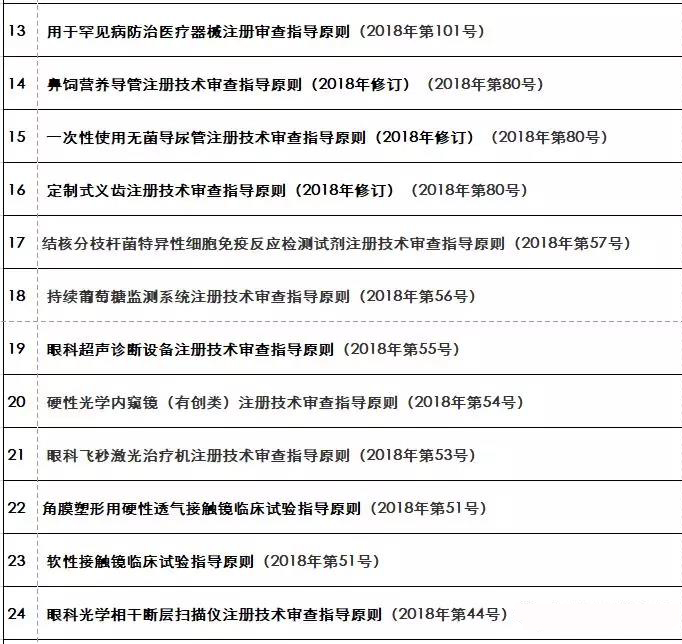
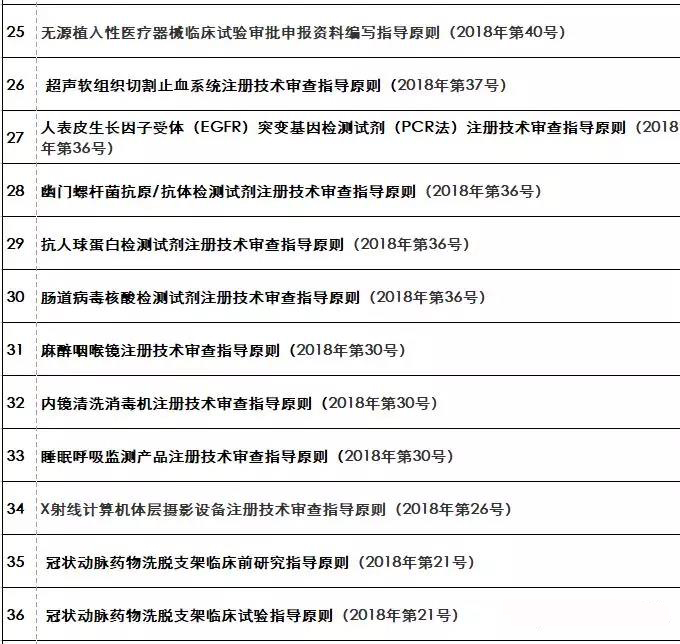
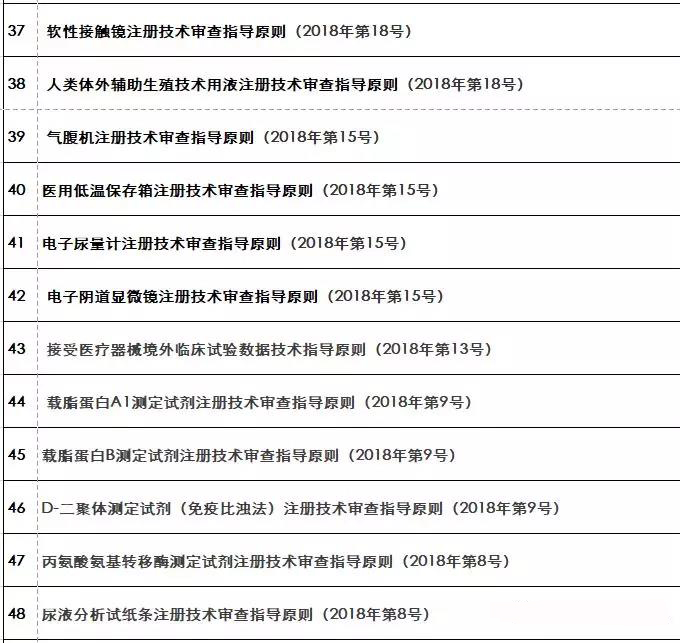
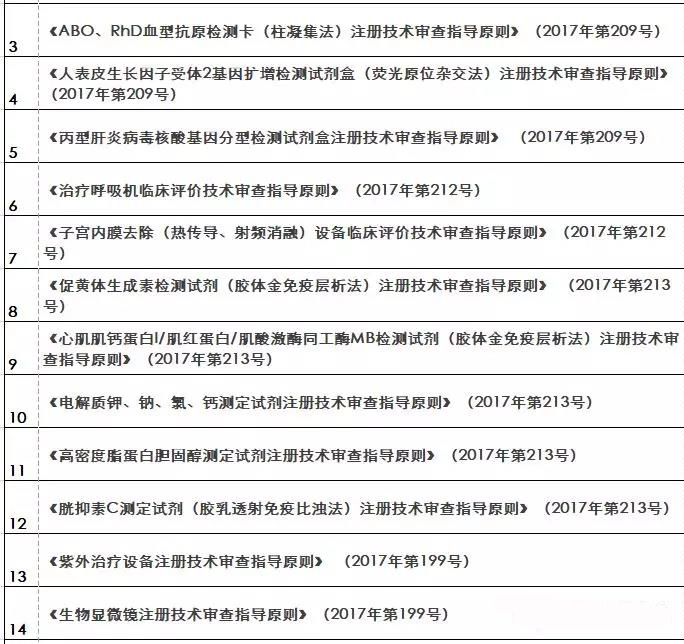
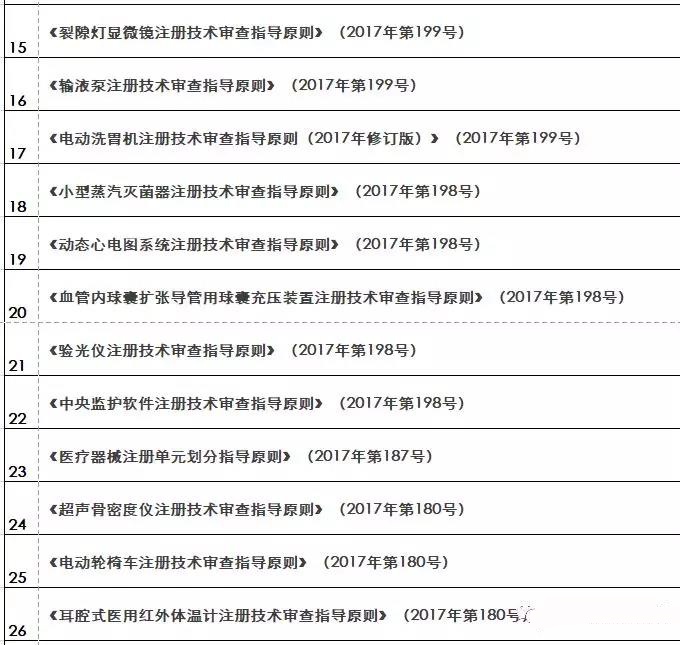
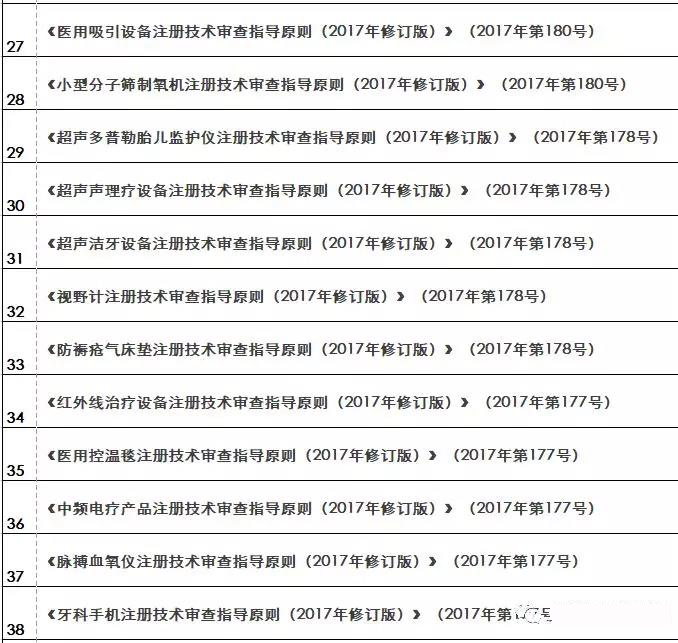
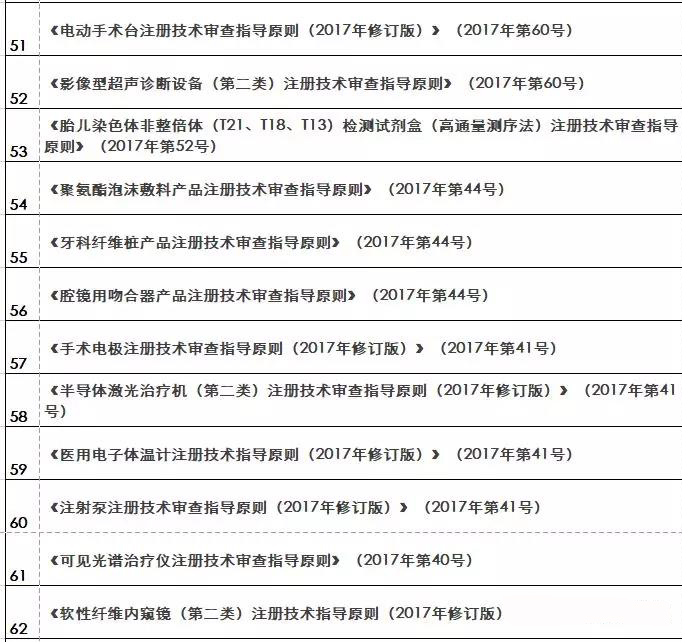
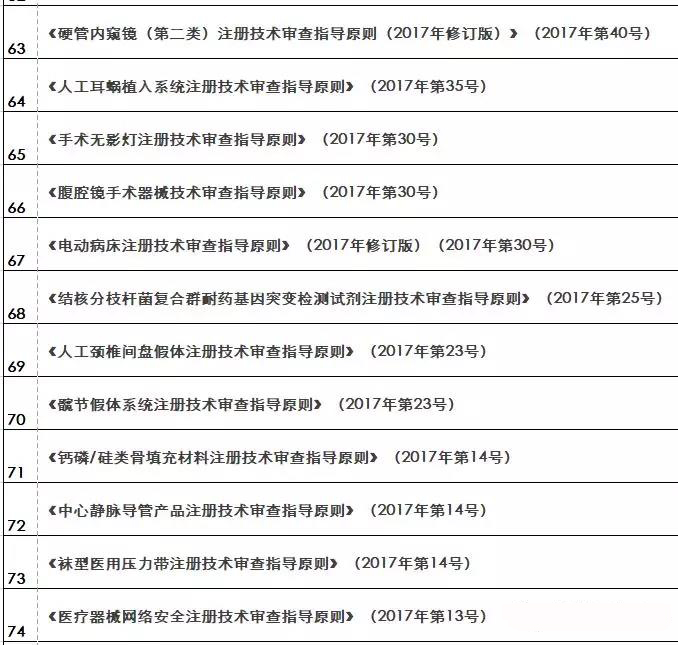
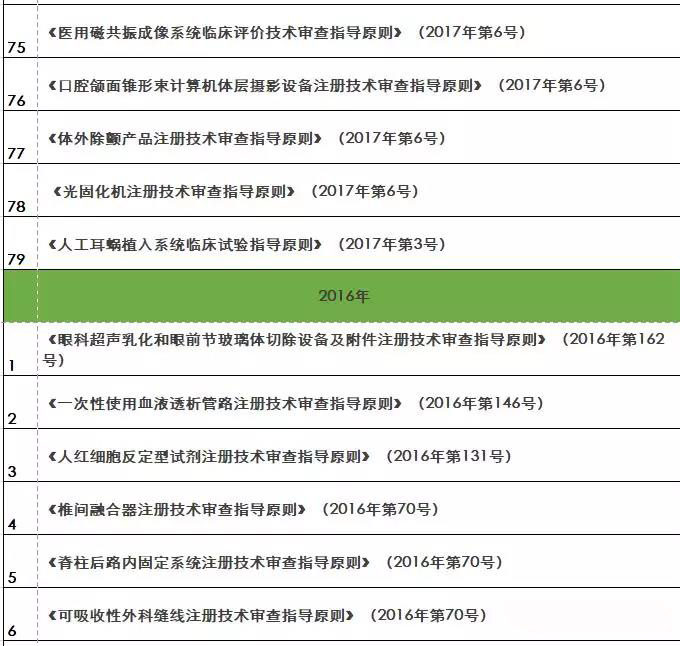
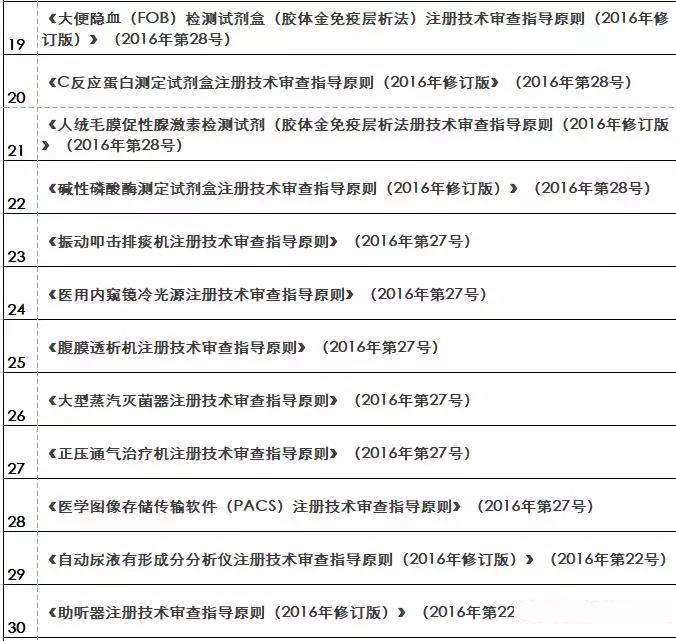
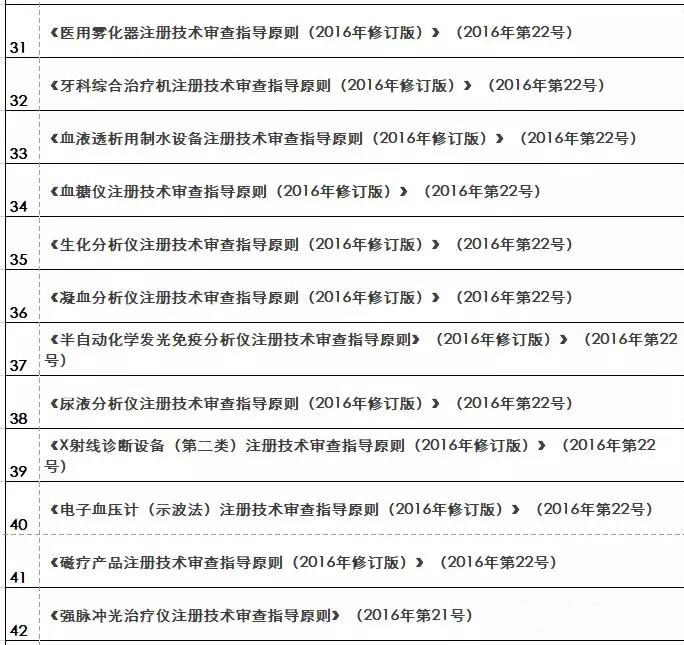
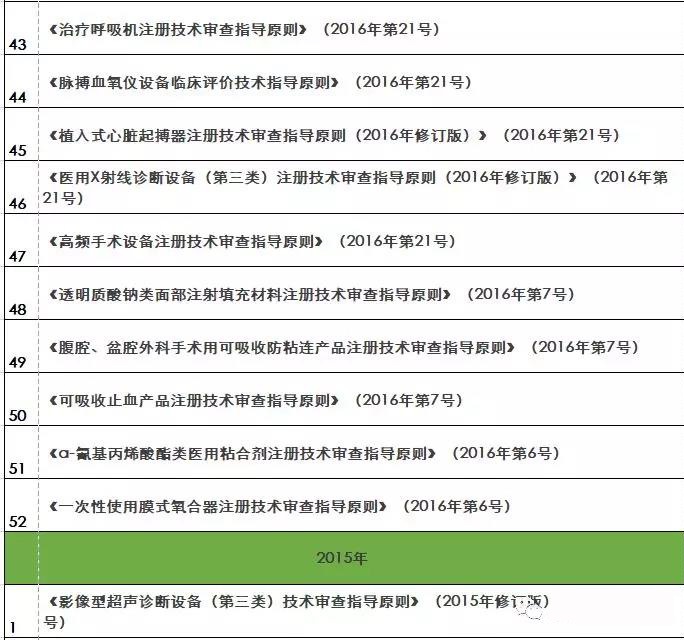
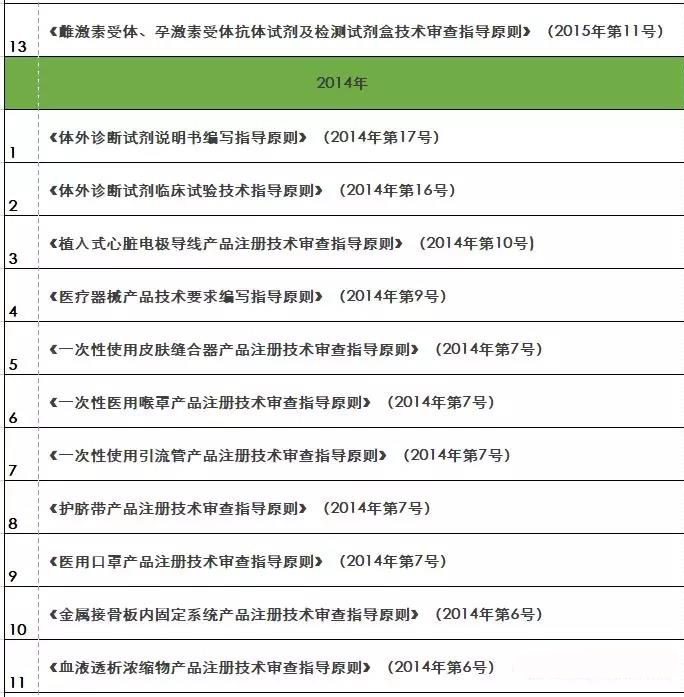
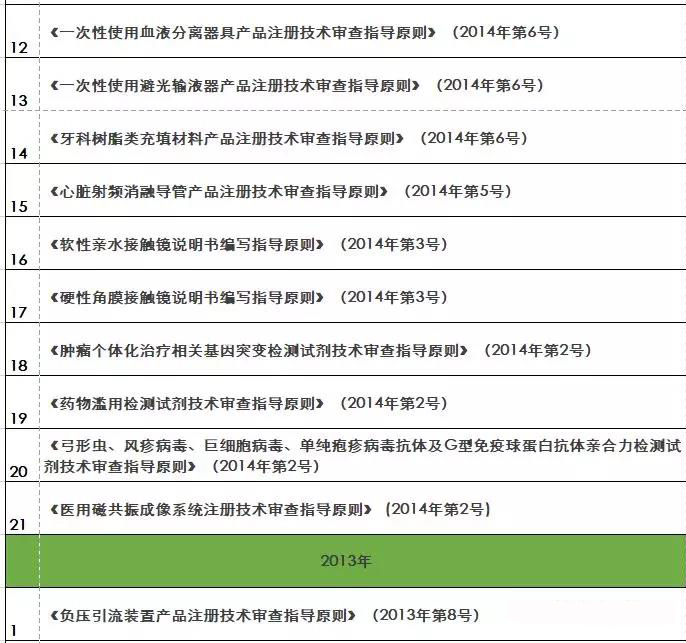
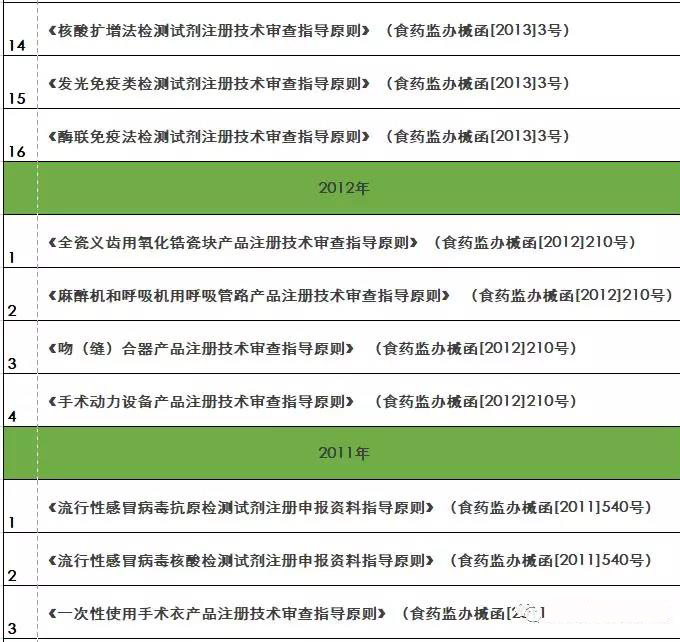
『重磅』2018年終大匯總!現(xiàn)行醫(yī)療器械注冊(cè)技術(shù)審查指導(dǎo)原則
文章出處:行業(yè)干貨 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時(shí)間:2019-11-02
隨著醫(yī)療器械在臨床上的廣泛應(yīng)用,產(chǎn)品的安全性和有效性越來越受到社會(huì)的關(guān)注。從醫(yī)療器械注冊(cè)檢驗(yàn)、臨床試驗(yàn)、體系
核查到最終注冊(cè)技術(shù)審查等環(huán)節(jié)都是產(chǎn)品進(jìn)入市場(chǎng)的必經(jīng)之路。要想保證產(chǎn)品最終能滿足技術(shù)評(píng)審的要求 之前,必須要有一個(gè)明確的方向及標(biāo)準(zhǔn)依據(jù) 指導(dǎo)原則(以下簡(jiǎn)稱“指導(dǎo)原則”)就是貫徹每個(gè)環(huán)節(jié)的主鏈條 那么指導(dǎo)原則的作用及其具體發(fā)布情況如何呢 01 技術(shù)指導(dǎo)原則的指導(dǎo)作用 指導(dǎo)原則其涉及的內(nèi)容正常包括:產(chǎn)品性能指標(biāo)的確定、注冊(cè)檢測(cè)要求 系核查關(guān)注重點(diǎn)等幾方面 指導(dǎo)原則是指導(dǎo)企業(yè)進(jìn)行醫(yī)療器械注冊(cè)申報(bào)的準(zhǔn)備及撰寫的規(guī)范性文件,也是指導(dǎo)各級(jí)器械審評(píng)部門開展工作的基礎(chǔ)資料和重要 依據(jù) 途徑。 02 指導(dǎo)原則適用性說明 提到指導(dǎo)原則 業(yè)能全部能滿足 理由及相應(yīng)的科學(xué)依據(jù)(不限于研究資料 也能說服現(xiàn)場(chǎng)體系核查人員及注冊(cè)技術(shù)評(píng)審人員 指導(dǎo)原則是對(duì)申請(qǐng)人和評(píng)審人員的指導(dǎo)性文件,不包括注冊(cè)審批所涉及到的行政事項(xiàng) 相關(guān)法規(guī)要求的其他方法,也可以采用 03 指導(dǎo)原則發(fā)布情況 本文收集了自2009年開始至今(2018年12.25) 其自2014年以來 從2009年-2018年的所有醫(yī)療器械技術(shù)審查指導(dǎo)原則